물리학에서 상(phase)은 일정한 물리적 성질을 가지는 균일한 물질계라고 합니다. 흔히 고체, 액체, 기체가 상에 해당하고, 이들 물질의 상태는 성질에 따라서 쉽게 구별할 수 있습니다.
고체는 일정한 모양과 부피가 있는 물질의 상태를 말합니다. 액체는 일정한 모양은 없으나 부피가 있는 물질의 상태를 말하고, 기체는 일정한 모양도, 부피도 없는 물질의 상태를 말합니다.
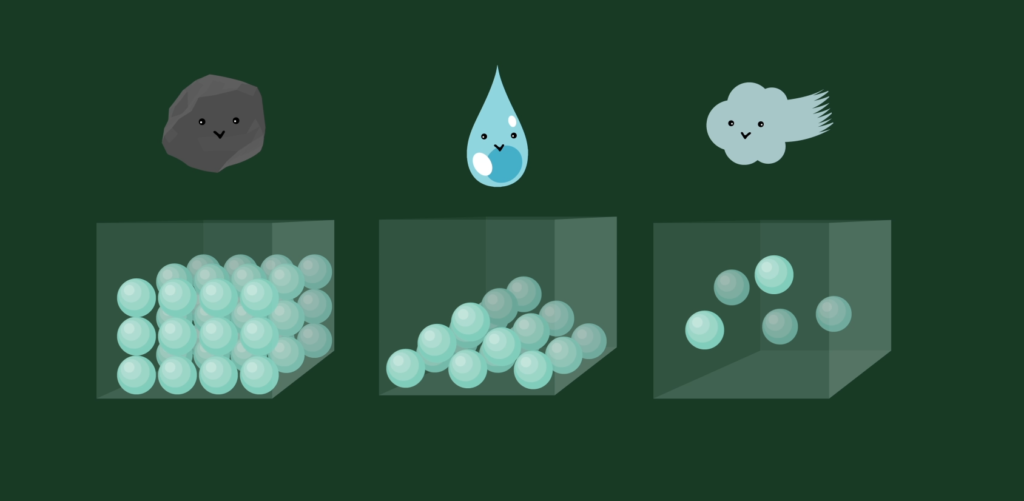
이와 같은 물질의 상태는 정해져 있다기보다는 주변 조건(예시: 얼음-물-수증기)에 따라 변합니다. 근데 불(fire)은 물질의 상태 중 어디에 속할까요? 기체라고 하기에는 모양과 부피가 있어 보이고, 고체라고 하기에는 일정한 모양과 부피가 아닙니다.
그렇다면 액체일까요? 불을 가만히 지켜보면 유동성이 있어 보입니다. 근데 아무리 봐도 액체와는 거리가 있습니다. 인터넷에 이와 관련한 자료를 찾아보면 많은 사람이 의문을 가진 주제입니다.
의문에 대한 답변을 보면 플라스마(plasma)라고 하는 사람도 있고, 기체라고 하는 사람도 있습니다. 일단 플라스마는 고체, 액체, 기체가 아닌 제4의 물질 상태를 말합니다.

기체 상태의 물질에 강력한 열이나 전자기장을 가하면 중성자와 전자, 이온 등의 입자로 이온화됩니다. 이온화된 상태의 입자 중 전기적으로 중성인 물질의 상태를 플라스마 상태라고 합니다. 근데 기체를 플라스마 상태로 만들기 위해서는 수천 도에서 수만 도의 열을 계속 가해야 합니다.
참고로 나무의 발화점은 400~470℃인데, 발화점만 넘기면 불이 발생하므로 우리가 일상생활에서 보는 불을 플라스마 상태라고 말하기에는 무리가 있습니다. 그렇다면 도대체 불은 뭘까요?
물질의 상태에 해당하는 게 없다는 말은 물질이 아니라는 이야기입니다. 불을 만들기 위해서는 물질이 타야 합니다. 이를 연소라고 하는데, 연소가 일어나기 위해서는 연료(물질)와 발화점 이상의 온도, 산소 등이 필요합니다.

해당 조건에서 하나라도 빠지면 연소 반응은 일어나지 않고, 불은 붙지 않습니다. 조건을 충족한다면 연소가 이루어지면서 불이 발생합니다. 불은 바로 이러한 연소 반응을 통해 에너지를 빛과 열의 형태로 방출하는 하나의 과정입니다. 즉, 물질의 상태가 아니라 에너지라는 겁니다. 궁금증이 해결되셨나요?
