냄비부터 놓고 물을 채워 넣은 다음에 불을 켜는 것이 먼저인 건 저도 알고 있습니다. 이다음에 할 일로 물이 끓은 다음에 면과 스프를 넣어야 하는지, 아니면 물이 끓기 전에 스프를 먼저 넣고 물이 끓을 때 면을 넣어야 하는지를 묻는 말입니다.
해묵은 논쟁으로 어떻게 먹을지는 먹는 사람 마음이라 간섭하고 싶지 않지만, 과학적인 이유에서 답변드리려고 합니다.
먼저 라면 봉지 뒤에 적힌 조리법에 따르면 물이 끓은 다음에 면과 스프, 후레이크를 같이 넣으라고 합니다. 이를 무시하고 스프를 먼저 넣어야 한다는 사람들의 주장에 따르면 크게 두 가지 이유가 있습니다.

하나는 스프를 먼저 넣으면 국물이 더 우러나 진한 맛을 느낄 수 있다는 주장과 또 하나는 물의 끓는점을 높여 고온에서 면을 익힐 수 있다는 주장입니다.
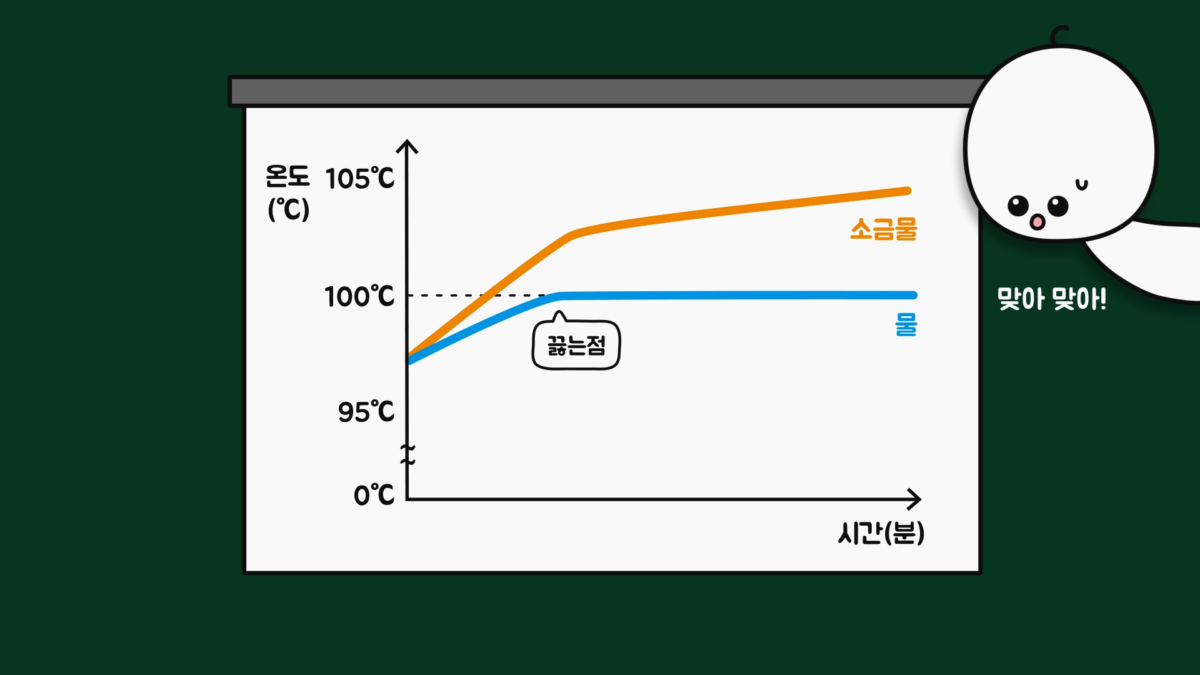
이 주장의 근거는 학교 수업 시간에 배운 끓는점 오름 현상인데, ‘대기압에서 물의 끓는점은 100℃이고, 소금 등의 이물질이 들어가면 끓는점이 높아진다’고 배운 적이 있을 겁니다. 그러니까 스프 속 소금 등이 이물질 역할을 해서 끓는점을 높일 수 있다는 논리입니다. 사실일까요?
끓는점의 변화를 계산할 수 있는 공식은 아래와 같습니다. 용매의 끓는점 오름 상수와 용질의 몰랄 농도, 반트호프 계수를 곱한 값이 끓는점 변화를 나타내는 공식입니다.
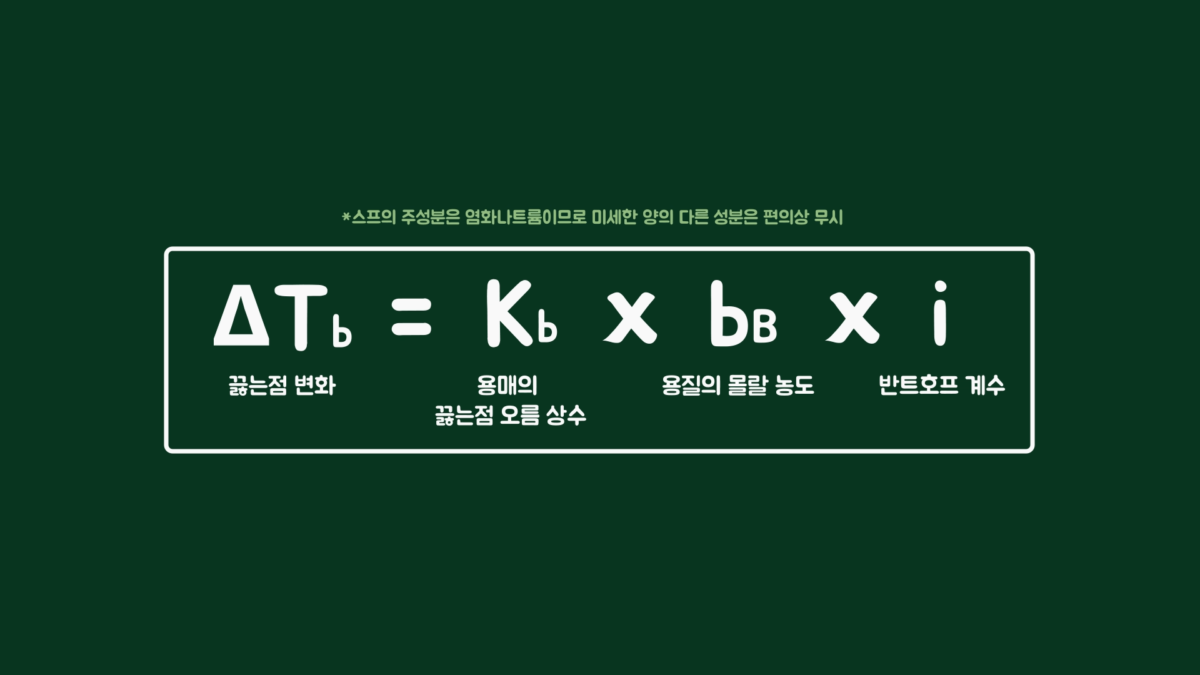
물의 끓는점 오름 상수는 0.512℃∙kg/mol로 정해진 값이고, 몰랄 농도는 용질의 몰수를 용매의 질량으로 나눈 값으로 mol/kg으로 표현됩니다. 그리고 몰수는 용질의 질량을 몰질량으로 나눈 값입니다.

라면마다 차이가 있으나 스프는 약 10g이고, 이중 염화나트륨은 약 2g 정도입니다. 염화나트륨의 몰질량은 58.44g/mol이므로 스프에 들어가는 염화나트륨 2g의 몰수는 위 식을 통해 구할 수 있고, 값은 0.034mol입니다. 이를 물 550g에 넣었을 때 몰랄 농도는 위 식으로 계산해 0.062mol/kg임을 구할 수 있습니다.
그리고 반트호프 계수(Van’t Hoff factor)는 용질이 용해될 때 몇 단위로 작용하는가를 표현하는 값인데, 염화나트륨과 같이 수용액 상에서 완전히 이온화되는 용질은 이상적으로 2의 값을 가집니다.

따라서 끓는점의 온도 변화를 구하는 식을 정리해보면 위와 같이 나오고, 물에 스프를 넣고 끓였을 때 끓는점이 0.063℃가 오른다는 것을 알 수 있습니다.
혹여나 라면 스프에 들어가는 염화나트륨을 2g으로 가정한 것에 이의를 제기하는 사람이 있을 수 있어서 스프 10g 전부가 염화나트륨이라고 가정해보고 계산해보겠습니다. 보다시피 0.315℃밖에 오르질 않으므로 스프를 넣어서 물의 끓는점을 높이겠다는 것은 어렵습니다.

그래도 무슨 상관이냐며 스프부터 넣겠다는 사람이 있을 텐데, 안전을 위해서라도 면을 먼저 넣는 것을 권장합니다. 사실 조리법에는 아래와 같은 경고 문구가 나옵니다.

왜냐하면, 물이 끓기 직전에 스프를 넣게 되면 갑자기 막 끓어 넘치는 현상을 보이기 때문입니다. 화학에서는 이물질 등의 유입으로 인해 핵이 형성되어 갑자기 끓어오르는 현상을 돌비현상(bumping)이라고 합니다.
이는 끓는점이 오르고 내림에 상관없이 끓을 준비가 거의 다 된 상태에서 스프가 구심점 같은 핵 역할을 하여 끓는 것을 촉발해 나타나는 현상입니다.

스프를 미리 넣어놨으면 괜찮겠으나 끓기 직전에 넣는 행동은 위험할 수 있으니 삼가길 바랍니다. 그리고 같은 이유로 전자레인지를 이용한 물 끓이기도 조심해야 합니다. 이론상 대기압에서 물의 어는점은 0℃이고, 끓는점은 100℃이지만, 무조건적인 내용은 아닙니다.

특히 전자레인지의 마이크로파를 이용하는 경우 100℃가 조금 넘어도 끓지 않고 평온한 상태를 유지할 수 있어서 이때 약간의 충격을 가하면 갑자기 끓어오르는 돌비현상이 나타날 수 있어서 조심해야합니다. 궁금증이 해결되셨나요?
– 원고 : ‘개와 고양이의 물 마시는 법‘의 저자 송현수(서울대학교 대학원 기계항공공학부 박사)
Copyright. 사물궁이 잡학지식. All rights reserved
